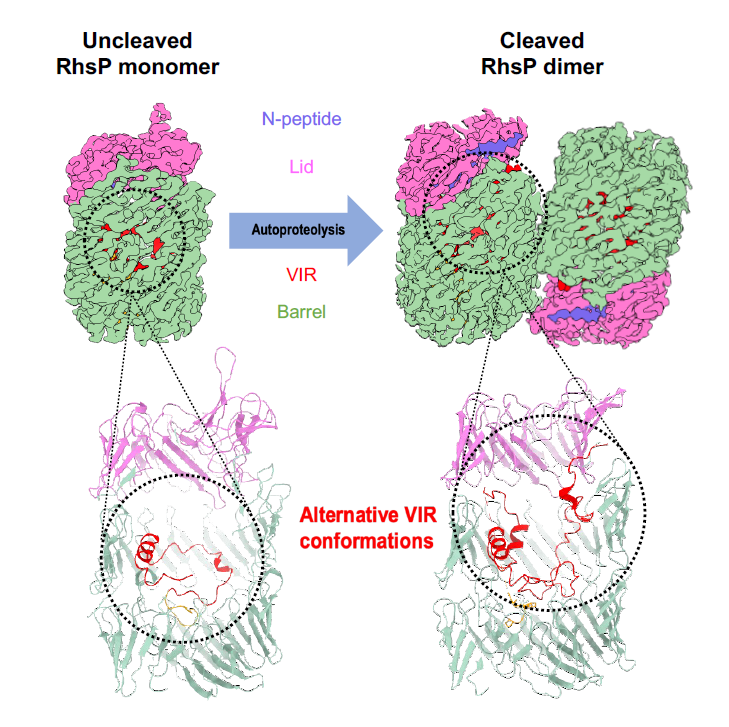
 肠炎弧菌毒素RhsP之自水解促使其毒素二聚化,这过程对肠炎弧菌攻击邻菌起关键作用
肠炎弧菌毒素RhsP之自水解促使其毒素二聚化,这过程对肠炎弧菌攻击邻菌起关键作用
澳门大学健康科学学院副教授周昶行带领的研究团队发现一种新型的肠炎弧菌毒素RhsP,颠覆了人类对Rhs类毒素自水解和C端毒性部分释放机制的理解,为了解肠炎弧菌如何与人体内肠道菌群争夺生存空间和导致肠胃炎奠定了基础理论。相关研究成果已获国际知名期刊《细胞报导》(Cell Reports)刊登。
每年全球有24亿肠胃炎(Gastroenteritis)患者,其中主要感染途径之一是进食被肠炎弧菌(Vibrio parahaemolyticus)污染的海鲜。肠炎弧菌需要通过其6型分泌系统(T6SS)来释放毒素,攻击和杀死人体内肠道菌群(Gut microbiota),从而竞争肠道内的生存空间。周昶行的研究团队发现一种新型的肠炎弧菌毒素RhsP,该毒素通过T6SS二型释放到邻近细菌体内,抑制并杀死邻菌,而肠炎弧菌自身则会制造免疫蛋白RhsPI来中和其毒素之毒性,避免自我杀害。RhsP是一个庞大的毒素蛋白,共有1381个胺基酸,总份子量为157kDa,该毒素以一个巨大的β桶结构为主体,桶内则有重要的自水解(Autoproteolysis)功能部分。
研究团队获中国科学院上海同步辐射光源支持,利用结构生物学技术揭示了肠炎弧菌RhsP毒素C端之毒性部分(RhsPC)和RhsPI免疫蛋白复合体的蛋白晶体结构,并解释免疫蛋白中和毒性和避免病菌自杀之份子机制,此结构是第一个在澳门以X光晶体学技术揭示的新型蛋白结构。
此外,研究队伍与中国科学院广州生物医药与健康研究院(GIBH)研究员何俊的团队合作,利用世界领先的冷冻电子显微镜和基因诱变技术,把RhsP毒素锁定在自水解之前和之后的型态,并以冷冻电子显微镜揭示各型态之份子结构。团队发现自水解会导致RhsP毒素二聚化(dimerization),揭示了毒素透过自水解改变份子结构来释放C端毒性部分之机理,而这对于肠炎弧菌攻击邻菌起到了关键作用。该结构是第一个在澳门利用冷冻电子显微镜技术揭示的新型蛋白结构。
是次研究的通讯作者为周昶行、何俊和前澳大健康科学学院副教授郑军。前澳大健康科学学院博士后唐乐和Nadia Rasheed、澳大健康科学学院博士生胡巧颖、中国科学院广州生物医药与健康研究院博士生董淑琪和实验室助理周宁坤为第一作者。该项目由澳门特别行政区科学技术发展基金(檔案编号:0009/2018/A1、0058/2018/A2、0113/2019/A2和0032/2021/A1)和澳门大学(檔案编号:MYRG2018-00221-FHS和MYRG2019-00050-FHS)资助。研究文章全文可浏览https://www.cell.com/cell-reports/fulltext/S2211-1247(22)01610-2