 智慧光动力诊疗剂设计示意图及多模态分子影像
智慧光动力诊疗剂设计示意图及多模态分子影像
澳门大学在医学分子影像和肿瘤精准诊疗方面取得新进展,有关团队开发了一种具多模态分子影像造影功能、近红外光激发的光动力诊疗剂,有助提高光动力治疗深层肿瘤的精准度,改善治疗效果。研究获国际生物材料领域的最顶级期刊《生物材料》(2018影响因数:10.273)刊登。
研究课题为《基于抑制肿瘤氧代谢并同时产生氧的肿瘤智能光动力诊疗》,由澳门大学健康科学学院副教授袁振的团队与深圳大学教授屈军乐的课题组合作。肿瘤光动力疗法(PDT)是基于氧、光敏剂和可见光为基础的、低副作用的无创癌症治疗手段,但传统的PDT采用紫外光或白光照射,其组织穿透表浅,通常只能用于皮肤癌的治疗;而将其用于其它深层组织的肿瘤的治疗,则受深层组织内肿瘤定位不准确、激发光穿透无法达到、深组织内肿瘤乏氧等关键问题的长期困扰。
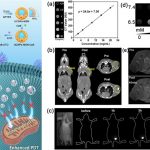
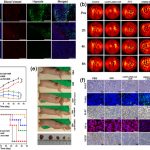
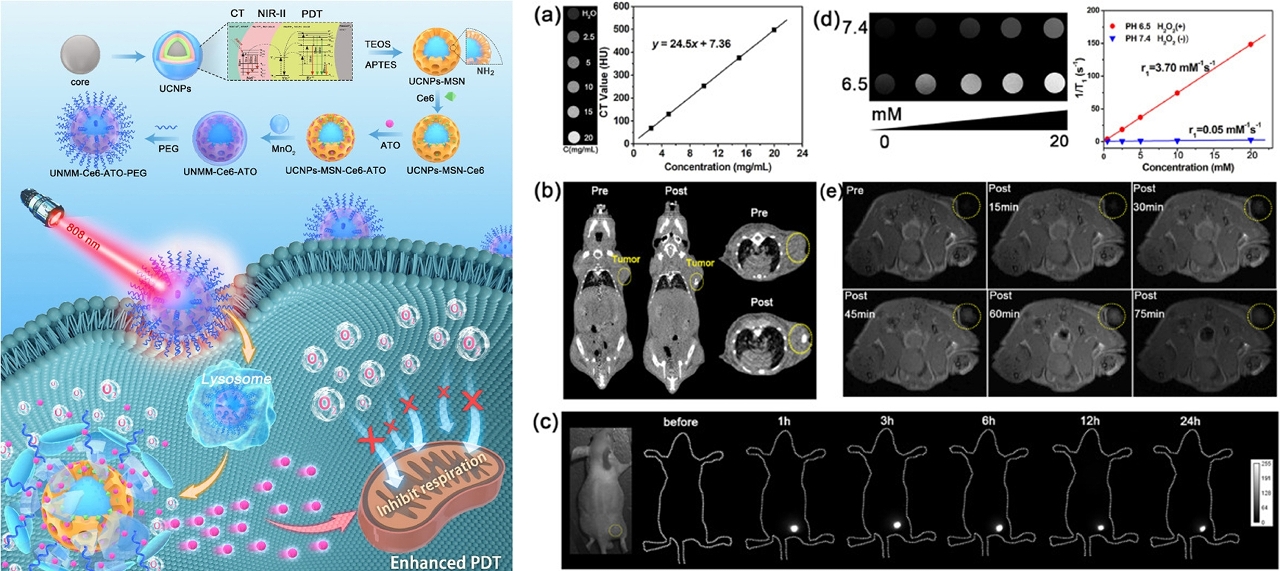
袁振副教授的研究团队针对肿瘤光动力诊疗难题,开发出复合智慧光动力诊疗剂,该多功能智慧药物具备(1)MRI、CT分子成像和近红外二区(1300nm)萤光分子成像能力,可定位深组织内肿瘤;(2)将808 nm近红外光转化为可见光激发光敏剂,实现深组织治疗;(3)肿瘤部位智慧释放肿瘤呼吸抑制剂,改善肿瘤乏氧,进一步促进光动力精准治疗。
研究人员通过多模态分子影像、共聚焦、细胞活测定等生物学实验和动物模型验证其疗效,并探索这种新型智慧光动力诊疗剂诱导肿瘤细胞死亡的生物学效应及其分子机制。研究发现,这种新型光动力诊疗剂为更广泛的深组织光动力疗法开辟了研究道路,具有非常重要的潜在临床应用价值,也为今后开发新的肿瘤临床治疗策略和光敏药物制剂提供一个新途径。
是次研究由袁振教授主导,主要参与者为其课题组研究助理王丹、薛彬、刘玉滨及博士生徐孟泽。另外,研究得到澳门大学(檔案编号:MYRG2019-00082-FHS, MYRG2018-00081-FHS)及澳门科学技术发展基金(檔案编号:025/2015/A1, 0011/2018/A1)的资助。全文可浏览:
https://www.sciencedirect.com/science/article/pii/S0142961220303343?via%3Dihub。