 研究团队运用全外显子测序技术揭示了肿瘤的进化过程
研究团队运用全外显子测序技术揭示了肿瘤的进化过程
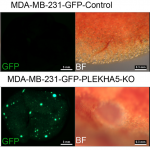
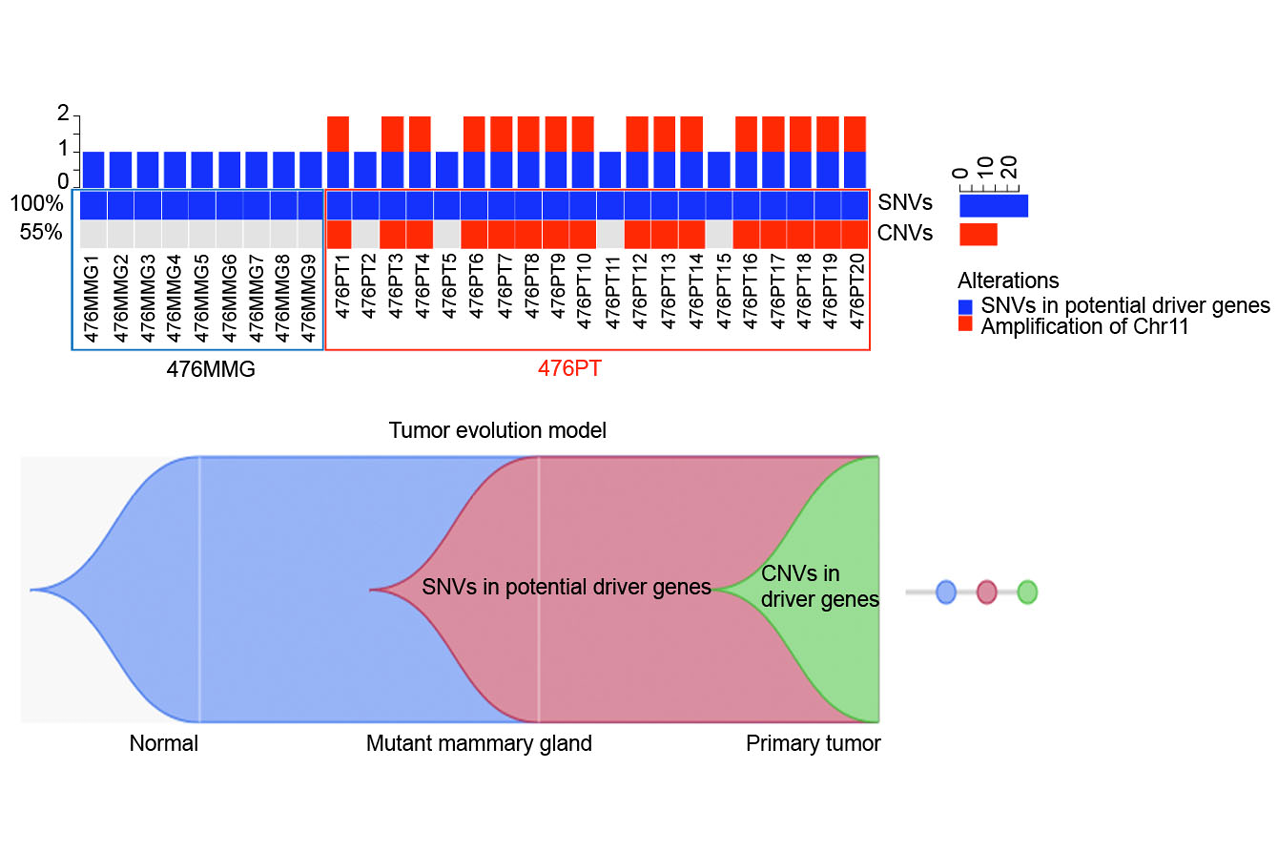
澳门大学健康科学学院副教授徐晓玲的研究团队运用全外显子测序技术,同时对BRCA1缺陷的乳腺组织和肿瘤进行了单细胞的单核甘酸突变和拷贝数变异分析,揭示了肿瘤的进化过程。研究团队更发现了一个新的乳腺癌转移抑制基因PLEKHA5,这个基因的缺失会促进乳腺癌的转移,是乳腺癌领域的一个重要发现。这项研究成果已在全球着名学术期刊《自然通讯》(Nature Communications)上发表。
乳腺癌易感基因BRCA1突变是大约四分之一的人类家族性遗传乳腺癌的起因,带有BRCA1基因遗传性突变的女性在其一生中患乳腺癌的风险高达40-80%。说到癌症,每个病人,甚至来源同一个病人的不同肿瘤的驱动事件都有可能是不一样的,这需要进一步的研究阐明。目前BRCA1缺陷的乳腺癌的起始,以及其怎样从早期的癌变前阶段一步步恶变、进化、发展、转移的生物学机制和原理尚不完全清楚。近年来,单细胞全外显子测序技术已经成为了一个强有力的工具去破译肿瘤的瘤内异质性,并鉴定癌症的驱动因子。但是,目前同时分析来自同一个细胞的单核甘酸突变和拷贝数变异仍极具挑战性。
为了理解BRCA1缺陷的乳腺癌的基因突变特征、进化过程、以及鉴定其肿瘤驱动事件,该研究团队运用全外显子测序技术,同时对BRCA1缺陷的乳腺和肿瘤进行了单细胞的单核甘酸突变和拷贝数变异分析,并用基因编辑工具CRISPR-Cas9对候选的驱动基因进行了体外和体内的功能验证。该研究有以下重要发现:1. BRCA1-缺陷的肿瘤进化起始于癌变前带有单核甘酸突变驱动基因的细胞,随着染色体通过自然选择不断累积癌症驱动基因的拷贝数变异,肿瘤发生进一步的恶化、生长、转移。2. 在每个不同的肿瘤内,这些突变是随机事件,可以影响很多癌基因,从而导致每个肿瘤独特的基因突变特征和病理特征。3. 当癌症或者转移的驱动事件发生在恶化前或者在低频率的时候,由于瘤内异质性的原因,组织块测序其很有可能检测不到这些低频事件,但单细胞可以测序可以解决这一问题。4. PLEKHA5就是这样一个例子,其突变存在于一小部分原位肿瘤细胞,但是在肝转移的肿瘤中占据了主导地位。5. CRISPR-Cas9介导的功能验证实验证明PLEKHA5不影响原位肿瘤的生长,然而它的缺陷可以促进肿瘤的肝转移和肺转移,说明它是一个癌症转移抑制基因。
这项研究由徐晓玲主导,博士研究生刘建林为第一作者。健康科学学院讲座教授邓初夏、副教授黄冠豪、研究助理教授苗凯、研究助理Ragini ADHAV和博士研究生舒适文也为该研究做出了重要贡献。该研究得到了澳门大学(檔案编号:MYRG2016-00138-FHS、MYRG2017-00088-FHS、 MYRG2019-00064-FHS)和澳门特别行政区科学技术发展基金(檔案编号:027/2015/A1、 029/2017/A1、 0101/2018/A3、0011/2019/AKP)的资助。