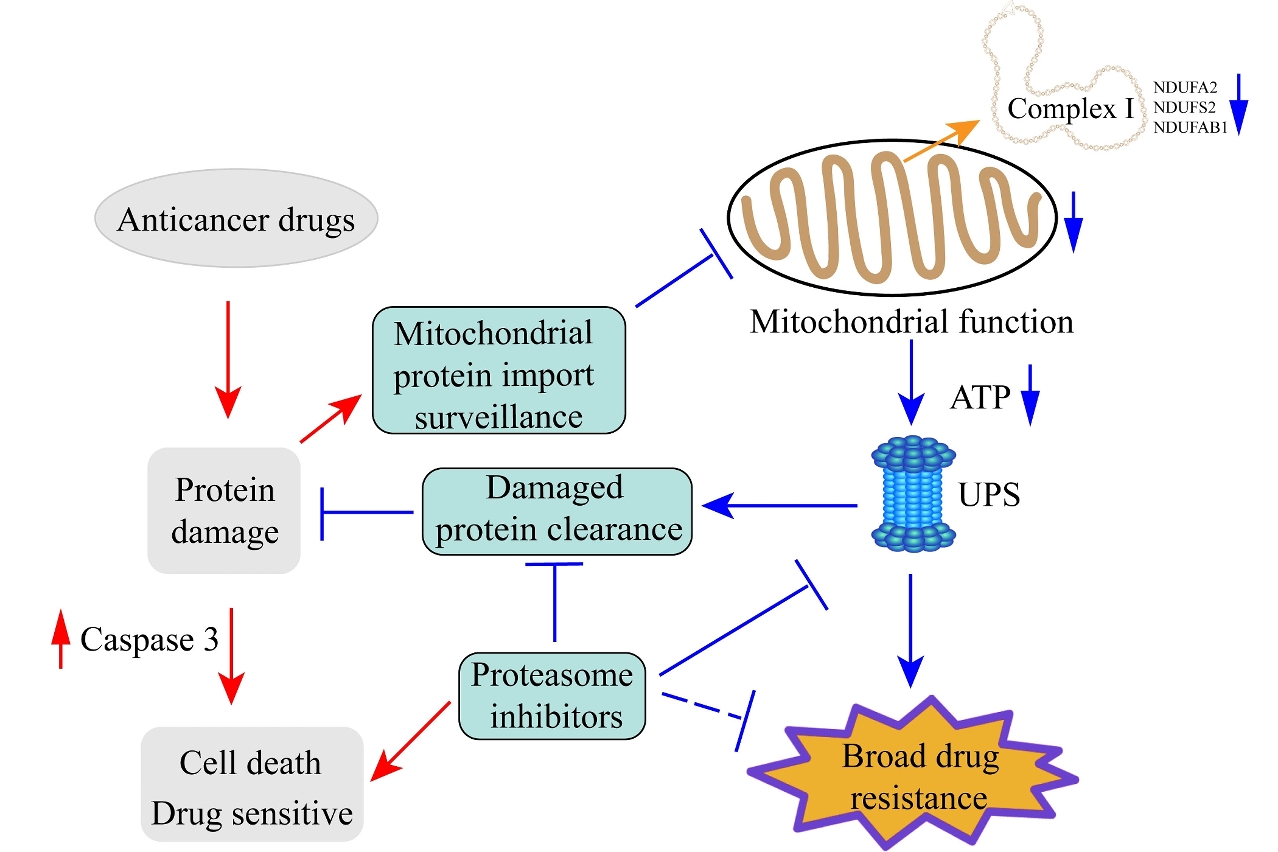
 抑制蛋白酶体的活性可以阻断多种类型癌症的广谱耐药性
抑制蛋白酶体的活性可以阻断多种类型癌症的广谱耐药性
澳门大学健康科学学院院长邓初夏领导的研究小组发现了泛素化蛋白酶体系统与药物耐受之间的联系,研究显示通过抑制蛋白酶体的活性可以阻断多种类型癌症的广谱耐药性。相关研究成果有助解决癌症病人的耐药性问题,已获国际知名期刊《先进科学》(Advanced Science)刊登。
癌症死亡率一直居高不下的重要原因是因为人体会自动对药物产生耐药性,当癌细胞同时或依次用几种药物治疗时,它们可能会变成多药耐药性,致使这类癌症非常难以治疗,例如肿瘤细胞原发性耐药、获得性耐药等。许多肿瘤即使在化疗处理初期效果很好,但是细胞会逐渐获得耐药性而得不到控制。此外,许多癌症在经一种药物治疗后,往往演变成对其它许多未接触过而且结构不同、作用机制各异的药物也产生交叉耐药性,即广谱耐药性,令许多尖端医疗机构束手无措。研究小组通过全基因组RNAi筛选和进化耐药模型,发现增强的蛋白酶体活性和较低的线粒体活性促进了顺铂耐药性。顺铂是目前临床应用最广泛的化疗药物之一,用以治疗各种不同类型的癌症。进一步的研究表明,顺铂治疗可引起蛋白质损伤,从而触发线粒体蛋白质输入监测通路的启动。线粒体蛋白输入监测通路的启动一方面导致线粒体活性的降低,另一方面能够启动蛋白酶体活性,从而增加受损蛋白的清除率并拯救细胞活力。另外,研究团队通过比对69种药物文库的筛选和患者类器官的筛选,证实增强的蛋白水解作用和较低的线粒体活性是耐受多达40种抗癌药物的共同机制,而蛋白酶体抑制剂治疗逆转了对其中27种药物的耐受性。研究成果进一步显示,通过纳米颗粒包备的顺铂和硼替佐米可以进一步增强了抗肿瘤的功效,并减轻了药物联合治疗引起的副作用。
研究团队在通过全基因组RNAi筛选来鉴定可能与耐药有关的所有人类基因时共发现45个基因与顺铂耐药有关,104个基因与顺铂敏感有关。他们使用多种模型展示了靶向这些候选基因所参与的细胞功能能够克服广谱耐药性。这些研究表明尽管不同的抗癌药物具有不同的结构,细胞靶标和作用机制,但癌细胞会启动相似的防御系统以维持细胞存活。研究证明增强的蛋白水解作用是这些耐药性的常见机制之一,而通过靶向这一通用的防御系统,能够逆转多种药物的耐受。这些发现在转化医学中具有重要意义。
这项研究由健康科学学院院长邓初夏领导,博士生邵方元为第一作者,镜湖医院和山顶医院亦参与部份研究工作。相关研究由澳门特别行政区科学技术发展基金资助(檔案编号:094/2015/A3, 048/2019/A1和0011/2019/AKP)和澳门大学资助(檔案编号:CPG2020-00004-FHS、MYRG2016-00139-FHS、MYRG2016-00132-FHS和MYRG2017-00113-FHS)。全文可浏览:https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202001914