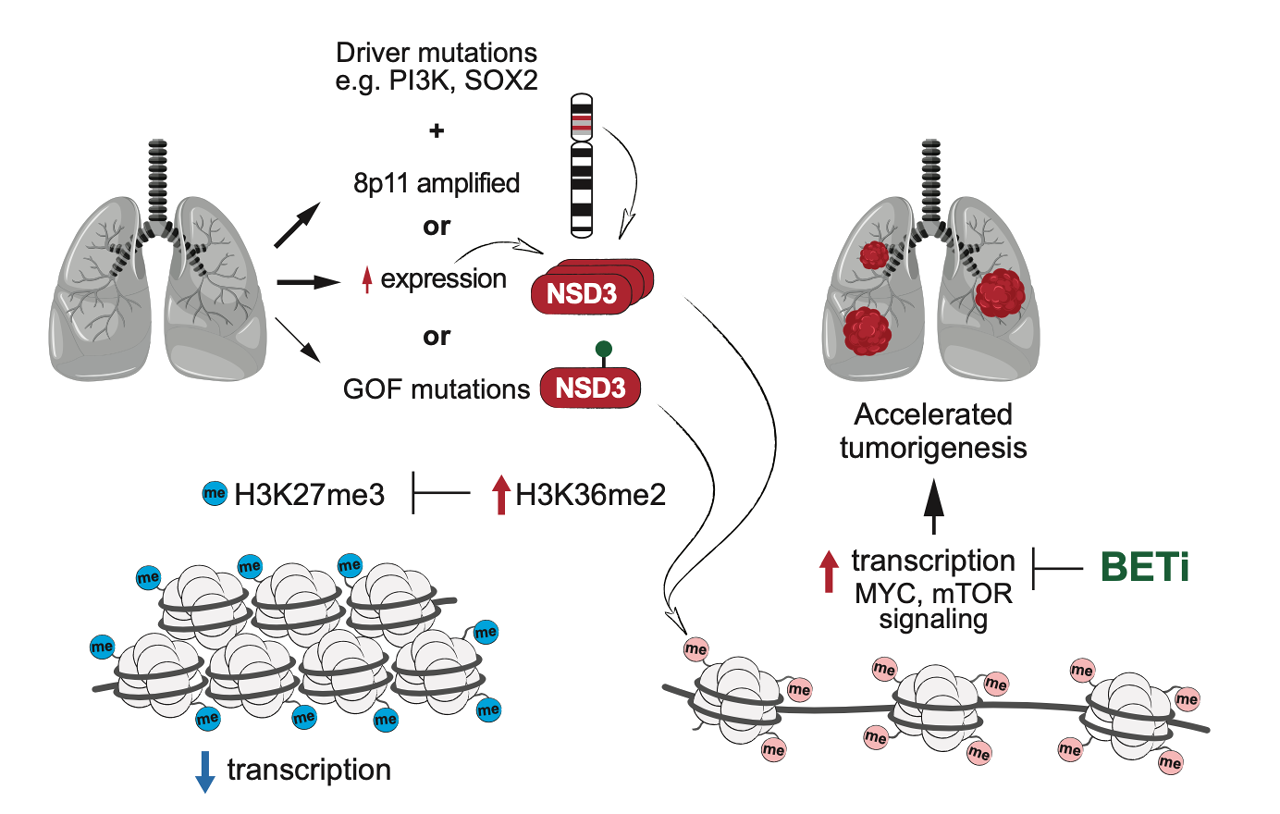
 NSD3蛋白參與肺鱗狀細胞癌的腫瘤發生過程,並可能是治療肺鱗狀細胞癌的有效靶點。
NSD3蛋白參與肺鱗狀細胞癌的腫瘤發生過程,並可能是治療肺鱗狀細胞癌的有效靶點。
澳門大學健康科學學院、史丹福大學和安德森癌症中心合作,在肺癌研究中取得突破。研究團隊發現NSD3蛋白參與肺鱗狀細胞癌的腫瘤發生過程,並揭示了NSD3可能是治療肺鱗狀細胞癌的有效靶點,是一項里程碑式的新發現。該研究成果已於國際著名期刊《自然》(Nature)上發表。
肺癌分為小細胞肺癌和非小細胞肺癌兩大類,後者主要包括腺癌、鱗狀細胞癌與大細胞癌三種類型。非小細胞肺癌的生長較緩,轉移也較慢,但可經開刀治療的早期病例僅約四分之一,術後仍可能發生轉移或復發,所以肺癌之治療方法仍有許多進步空間。史丹福大學(Stanford University)人文與科學學院生物系、安德森癌症中心(MD Anderson Cancer Center)與澳大的聯合團隊揭示了NSD3促進肺鱗狀細胞癌腫瘤發生的內在分子調控通路,該機制的發現推翻了之前人們對8號染色體確切癌症驅動基因的推測,更重要的是為肺鱗狀細胞癌的治療提供了新的潛在治療靶點。
在之前對肺鱗狀細胞癌的研究中,人們發現8號染色體的特定區域的擴增會促進肺鱗狀細胞癌的發生。一開始,主要的候選癌症驅動基因是FGFR1蛋白,但是嘗試將FGFR1蛋白作為抑制靶點的臨床實驗並不成功。但是研究人員發現H3K36甲基轉移酶NSD3,也位於8號染色體該區域。且以小鼠作為模式生物,隨著NSD3的敲除,減緩了腫瘤的生長,並延長了小鼠的生存期。研究人員還發現一個該型腫瘤患者常見的NSD3遺傳突變,在體內和體外都能增加組蛋白H3K36的催化活性。這個突變會引發NSD3催化變化,加速了小鼠模型的腫瘤發生,並降低了小鼠的總體生存率。這個突變會引發表觀遺傳的整體變化,促進致癌基因的更多表達。此項研究還發現,NSD3依賴的腫瘤可能對溴結構抑制劑敏感,具有潛在臨床價值。
是次研究由史丹福大學人文與科學學院生物系教授Or Gozani主導,澳大健康科學學院助理教授邵寧一為共同通訊作者。相關研究獲澳門特別行政區科學技術發展基金(檔案編號:0038/2020/AFJ)和澳門大學(檔案編號:SRG2019-00177-FHS)資助。全文可覽:https://www.nature.com/articles/s41586-020-03170-y